THEME1
Réactivité, Chimie Hétérocyclique et Applications :
L’activité scientifique de l’équipe EURECA est centrée principalement ces deux dernières décennies sur la génération et l’utilisation d’espèces cationiques en chimie hétérocyclique. Ces ions iminiums, thioniums, acyliums, et surtout N-acyliminiums obtenus généralement en milieu acide sont employés comme intermédiaires clés pour la synthèse de molécules appartenant aux familles d’alcaloïdes majeurs telles-que les protoberbérines, quinoléines, isoquinoléines, indolizines et aromathécines ainsi que des analogues ayant des applications pharmacologiques intéressantes, anticancéreuses notamment (Figure 1).
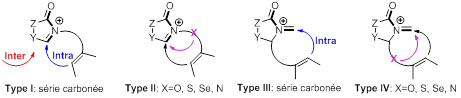
Figure 1. Exemples d’ions N-acyliminiums générés et utilisés.
L’Hétérocyclisation via un ion N-acyliminium, une nouvelle approche méthodologique
Différents modes de piégeages de ces intermédiaires réactionnels sont exploités aussi bien en version intermoléculaires qu’intramoléculaires. Celles-ci portent pour l’essentiel sur des réactions d’α-amidoalkylation seules ou plus encore en association avec de grandes réactions telles-que Grignard, Pummerer, transposition, hétérocyclisation et récemment la Métathèse. Dans ce registre si la formation de la liaison C-C par ce protocole est largement explorée par la communauté scientifique dont nous même en série racémique et chirale (Figure 1, espèces I & III), celui qui consiste en la formation d’une liaison C-X (X=hétéroatome ; Figure 1, espèces II & IV) émerge actuellement comme un nouveau champ d’application prometteur de cette chimie.
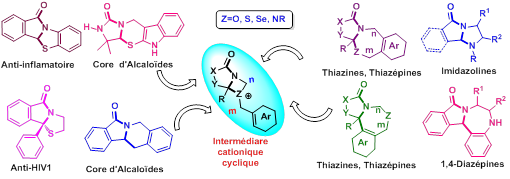
Figure 2. Exemples de squelettes obtenus par les processus d’hétérocyclisation.
L’Hétérocyclisation vs carbocyclisation, une nouvelle approche méthodologique
Parallèlement à ces processus d’hétérocyclisations qui ont pour cœur l’engagement d’un ion N-acyliminium dans un processus en tandem/domino, nous nous sommes intéressés également à des processus réactionnels impliquant en amont ou en aval des processus réactionnels impliquant la formation de liaisons C-C et C-X (avec X=hétéroatome). Lors de ces transformations, les processus utilisés reposent sur le couplage radicalaire ou par les sels métalliques tels que le cuivre, le ruthénium ou le palladium. Dans ce dernier cas, le réactif palladié joue parfois un rôle inattendu d’acide de Lewis.
Application de nos protocoles à travers quelques exemples de travaux récents :
Exemple d’une approche radicalaire
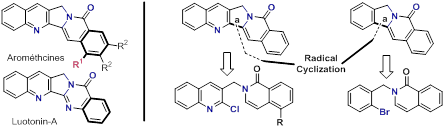
Exemple d’une approche ionique
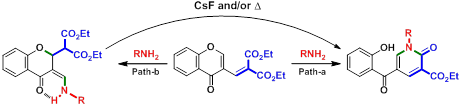
Exemple d’une approche tandem
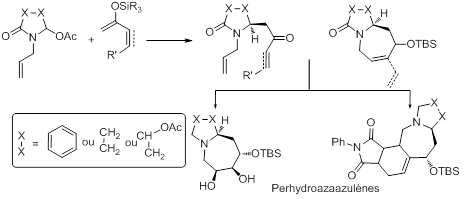
Quelques exemples de travaux en cours :
• Valorisation des réactions de cyclotrimérisation en tandem avec les ions N-acyliminiums catalysées par les sels du ruthénium, de fer et d’or.
• Elaboration de systèmes hétérocycliques de la famille des acétals mixtes par le piégeage des bis ions N-acyliminiums par les bis nucléophiles et hétéronucléophile.
• Accès aux pyridones fusionnées par activation à distance à l’aide du palladium.
• Utilisation des réactions d’a-amidoalkylation intermoléculaire en vue un accès rapide à des analogues contraints de la combrétastatine CA-4 naturelle inhibiteur puissant de la tubuline.
• Nouvelles plateformes azaindoliques potentiellement utiles pour la modulation en pharmacochimie.
• …
Mots Clés : Espèces Cationiques, α-Amidoalkylation, Cyclotrimérisation, Réactions Tandem, Activation (Cs, Bi, Au, Pd, Cu, Zr), Alcaloïdes, Aromathécines, Indolizines, Pyridones, Polyphénols, Antioxydants, Antitubuline, Anticancer.
THEME2
Synthesis of N-heterocycles using TANDEM/DOMINO reactions :
Our group is interested in the development of new tandem/domino reactions for the synthesis of polysubstituted N-Heterocycles found in many biologically relevant compounds. For that purpose, we have employed N-substituted α-bromoacetamides 2 or benzyl (2-bromoethyl)carbamate 3 together with Michael acceptors 1 as key partners. The aza-Michael induced ring closure (aza-MIRC) tandem process is usually highly diastereoselective and led to the formation of versatile pyrrolidin-2-ones 4 or pyrrolidines 5, respectively. This reaction is compatible with a wide variety of functional groups, and when started from selected Michael acceptors 1 bearing an alkoxy group (R2 = OMe or OEt) led to unprecedented N-acyliminium ion precursors in good yields. Straightforward syntheses of the tricyclic core of Martinellines 6 or Spirooxindoles 7 were achieved, these molecules known respectively for their anti-inflammatory and anti-tumor activities.
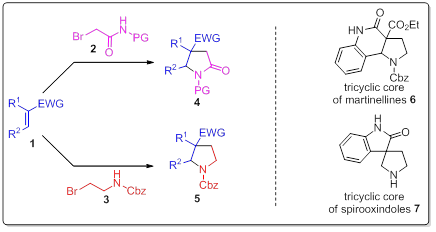
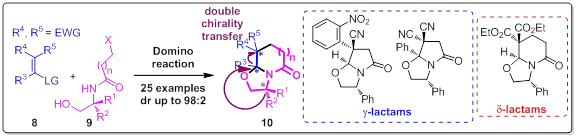
Moreover, a domino reaction starting this time from N-hydroxyalkyl α-bromoacetamides 9 and Michael acceptors 8 to access highly functionalized bicyclic γ- and δ-lactams 10 has been developed. This process allows the formation of two contiguous and fully controlled tertiary/quaternary and quaternary stereo-centers. When starting from (R)-phenylglycinol derived amides, the resulting enantioenriched lactams are obtained with low to good yield and high stereoselectivity. The origin of the double chirality transfer was studied via DFT calculations, in collaboration with Professor Arnaud Martel (Université du Mans), and has been attributed to a kinetic control by one of the two last steps of the sequence. The total synthesis of heterocyclic alkaloids using this methodology is currently under study.